原标题:科学家发现PD-1降解机制,助力肿瘤免疫治疗设计新方案
11月29日上午,澎湃新闻(www.thepaper.cn)从中国科学院生物化学与细胞生物学研究所(简称:中科院生化与细胞所)获悉,该所分子生物学国家重点实验室许琛琦研究团队首次揭示了人体免疫系统“刹车”分子PD-1的降解机制,相关论文29日凌晨在线发表在国际顶级学术期刊《自然》(Nature)上。

两位第一作者孟祥波(左)和刘希伟博士(右)和通讯作者许琛琦研究员(中)。
许琛琦表示,PD-1是肿瘤免疫治疗领域的明星分子,此前人们更多致力于研发其药物,但其团队该项研究阐明了PD-1的调新控机制,有助于研究人员更好地理解肿瘤免疫应答并设计新的肿瘤免疫治疗方法。
PD-1是最重要的药物靶点之一,针对PD-1的现有药物已开始应用于肺癌、肝癌、肾癌等10多种肿瘤的临床治疗中,但并非对所有的患者都有效。
PD-1的发现者Tasuku Honjo分享了2018年的诺贝尔生理与医学奖。此前的研究发现,部分肿瘤细胞会通过激活PD-1通路,从而逃避免疫细胞的攻击。而阻断PD-1通路的药物,可以恢复病人免疫系统的抗肿瘤功能,达到治疗目的。
在许琛琦团队的最新研究中,他们首先在正常的免疫T细胞中发现了PD-1的快速降解过程,随后鉴定出控制该过程的关键蛋白质分子FBXO38。
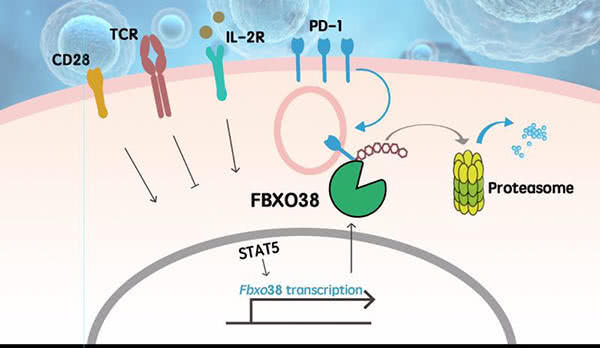
在被肿瘤“包围”的T细胞中,FBXO38“活跃”程度过低,这可能是PD-1不能被正常降解、数量堆积的重要原因。
许琛琦团队进一步发现白介素2可以恢复FBXO38的“活跃”度,让PD-1回归“正常指标”,从而恢复免疫系统的抗肿瘤功能。
白介素2已经是治疗黑色素瘤和肾癌的临床药物,但其副作用较大,未能在临床上广泛应用。许琛琦表示,该研究可以部分解释白介素2的抗肿瘤机制,今后可以继续优化白介素2的剂型/剂量或设计新的联合治疗方案。
此外,为什么被肿瘤“包围”后,T细胞中FBXO38“活跃”程度就降低了?许琛琦表示,他们团队正在寻找这一问题的答案。他认为,这一现象可能与表观遗传学调控等有关。
本研究主要由中科院生化与细胞所许琛琦研究组完成,博士研究生孟祥波和刘希伟为共同第一作者。在论文中做出贡献的还有多个科研团队,包括南方医科大学杨巍教授,中山大学魏来教授、周鹏辉教授,复旦大学医学院附属中山医院黄晓武教授,生化与细胞所刘小龙研究员和胡荣贵研究员以及美国MD Anderson癌症中心孙少聪教授。经费支持来自国家自然科学基金委、中国科学院、上海市科委以及中组部万人计划。
